
EXHIBIT 99.1

Rapport d’essais de l’appareil de prétraitement des déchets VKIN 300 selon les préconisations de la norme NFX 30503-1
Laboratoire Hygiène Hospitalière
CHU Clermont-Ferrand
Mai-Juin 2025
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 1 |
|
| ➢ | Essais sur la contamination microbienne aérienne (NFX 30503-1 Annexe A1) |
|
|
|
|
Méthodes
Prélèvement par biocollecteur Sampl’air (AES Laboratoires) étalonné le 20/10/2024.
Volume prélevé par échantillon : 100 litres par impaction sur géloses Trypcase Soy Agar (TSA) (Biomérieux, réf 43011).
Conservation et transports des prélèvements à 4°C jusqu’à mise en incubation (délai < 24h)
Gélose TSA incubée 3 jours à 30°C et 2 jours à 25°C
Expression en unités formant colonies / m3, conversion en log10.
Résultats
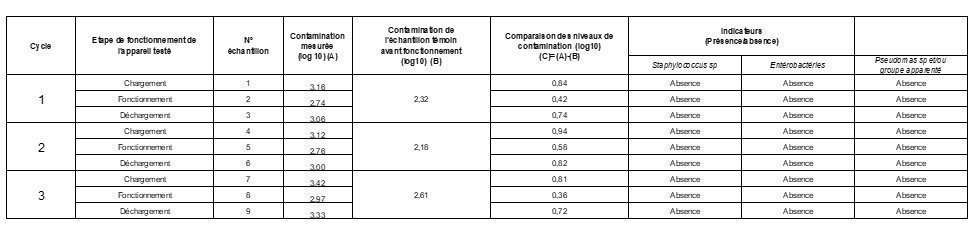
Absence de Staphylococcus spp, d’entérobactéries, de levures, de Pseudomonas spp et autres bacilles à Gram négatif non fermentaires
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 2 |

|
| ➢ | Essais de traitement sur indicateurs biologiques (NFX 30503-1 Annexe A2) |
Méthodes
Description des porte-germes
Porte-germe constitué de carré de compresses non-tissé (LCH ref 44564 Lot 4500005471)
|
| I. | Bacillus et Aspergillus |
Numération des suspensions bactériennes et fongiques
- Dilution des suspensions mères jusqu’à 10.-8 pour Bacillus et jusqu’à 10.-9 pour Aspergillus dans du bouillon tryptone sel
- Etalement de 100 µl des dilutions 10.-5 jusqu’à 10.-8 pour Bacillus sur gélose TSA
- Etalement de 100 µl des dilutions 10.-6 jusqu’à 10.-9 pour Aspergillus sur gélose Sabouraud (Thermo Scientific réf PO5096A)
- Incubation 48-72 h à 30°C
Dépôt des microorganismes sur les compresses porte-germes
- Bacillus : dépôt de 100 µl de la suspension bactérienne
- Aspergillus : dépôt de 10 µl de la suspension bactérienne
Ajout de sang de mouton comme substance interférente (Labmedical réf H04F-0817-P-0025) dans la suspension
Inoculation de la suspension par dépôt sur l’ensemble du porte-germe
Après traitement (indicateurs biologiques et courbe D)
Les compresses sont transférées dans des tubes Falcon stériles. On rajoute 3 ml (volume minimum pour que la gaze soit bien imprégnée) de bouillon Tryptone sel dans chaque tube. Vortexer 5 min.
Dilutions des suspensions
- compresses tube transport : dilution jusqu’à 10-7
- compresses indicateurs biologiques et courbes D : dilution jusqu’à 10-4
- étalement de 100µl des dilutions sur gélose TSA (Sabouraud pour Aspergillus). Le reste de l’échantillon pur est ensemencé sur des boites de Petri supplémentaires de façon à analyser l’ensemble de l’échantillon.
- Incubation 48-72h à 30°C
|
| II. | Adenovirus |
Culture des cellules HeLa
Le milieu utilisé pour la croissance des cellules est HeLa est le milieu MEM préparé comme suit :
MEM (450 mL) + 10% SVF décomplémenté filtré à 0.22 µm (50 mL) + ATB2x (1mL)
Virus : Human Adenovirus 5 (ATCC VR-5 TM) Lot 70053996 Date de validation 26/09/2022
Modalités de culture du virus
Les cellules HeLa sont ensemencées en microplaques 96 puits (Falcon, ref 353072) 48 h avant l’infection.
Les porte-germes sont placés de façon aseptique dans un tube Falcon contenant 3 mL de milieu MEM.
Sonication pendant 1 min (Branson 2510) puis vortex pendant au moins 2 min
Dilution de série 10 en milieu MEM
Inoculation des microplaques avec l’échantillon pur et les dilutions (100 µL par puits, 8 puits par dilution). Le reste de l’échantillon pur est ensemencé sur des puits supplémentaires de façon à analyser l’ensemble de l’échantillon.
Incubation 2h à 37°C en agitation douce puis ajout de 100 µL de milieu MEM.
Incubation à 37° C sous 5% de CO2
Lecture de l’effet cytopathogène à 2 et 3 jours post inoculation.
Détermination du titre viral selon la méthode de Spearman Kärber.
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 3 |

Références des produits utilisés pour les cultures cellulaires et virales :
MEM avec glutamine (réf Dutscher L0416 – 500)
PBS sans calcium ni magnésium (réf Dutscher L0615 – 500)
Trypsine avec rouge phénol sans calcium ni magnésium (réf Dutscher L0930 – 100)
Sérum de veau fœtal
Antibiotiques Pénicilline Streptomycine Néomycine (réf Sigma P4083)
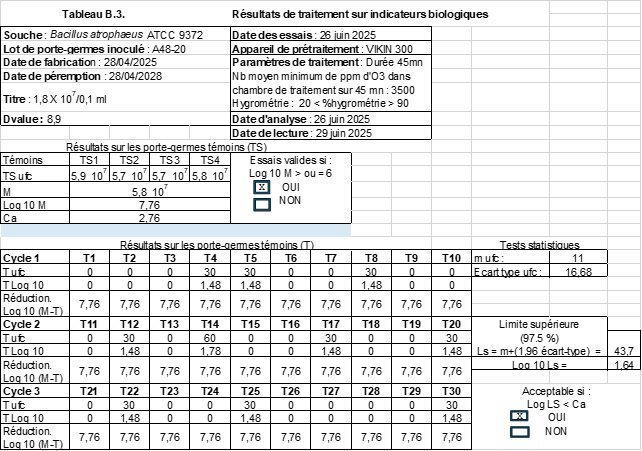
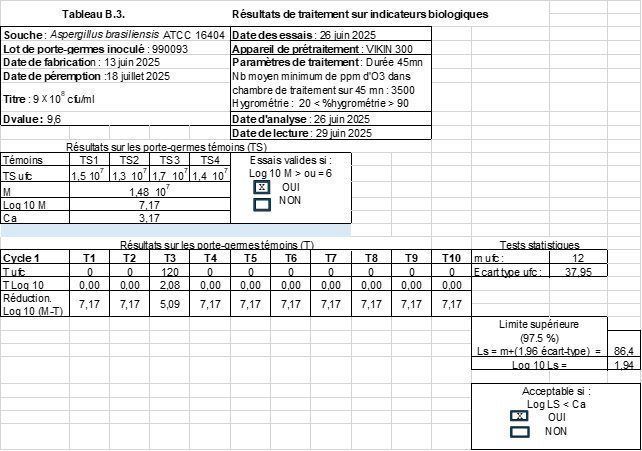
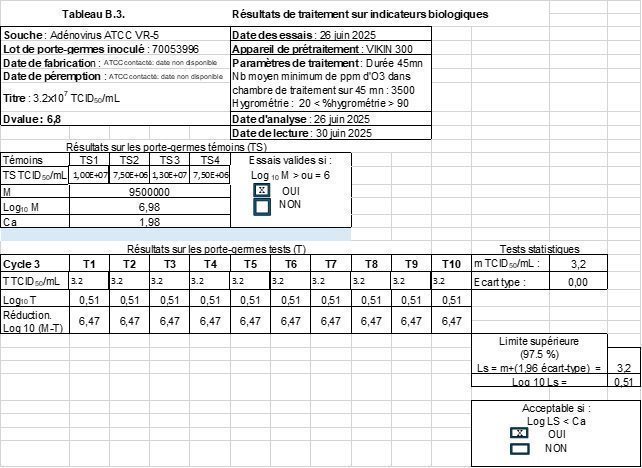
Résultats
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 4 |

| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 5 |

| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 6 |

|
| ➢ | Essais de traitement sur déchets infectieux et essais de reviviscence (NFX 30503-1 Annexe A3) |
Méthodes
Déchets avant traitement
- Peser 5 gr de DASRI
- Ajouter 45 ml de bouillon Tryptone sel (Dutscher réf 693424)
- Vortexer
- Laisser en contact à température ambiante pendant 1h en vortexant régulièrement
- Faire des dilutions jusqu’à 10-7 en bouillon tryptone sel
- Etaler 100 µl des dilutions 10.-4 jusqu’à 10.-7 sur des géloses TSA
- Incuber 48-72h à 30°C
- Numération de la flore bactérienne aérobie revivifiable et recherche de la présence de Staphylococcus spp, d’entérobactéries, de levures, de Pseudomonas spp et autres bacilles à Gram négatif non fermentaires
Déchets après traitement
- Peser 5 gr de DASRI
- Ajouter 45 ml de bouillon tryptone sel
- Laisser en contact à température ambiante pendant 1h en vortexant régulièrement
- Faire des dilutions de 10.-1 jusqu’à 10.-5 en bouillon tryptone sel
- Etaler 100 µl des 5 dilutions sur des géloses TSA
- Incuber 48-72 h à 30°C
- Numération de la flore bactérienne aérobie revivifiable et recherche de la présence de Staphylococcus spp, d’entérobactéries, de levures, de Pseudomonas spp et autres bacilles à Gram négatif non fermentaires
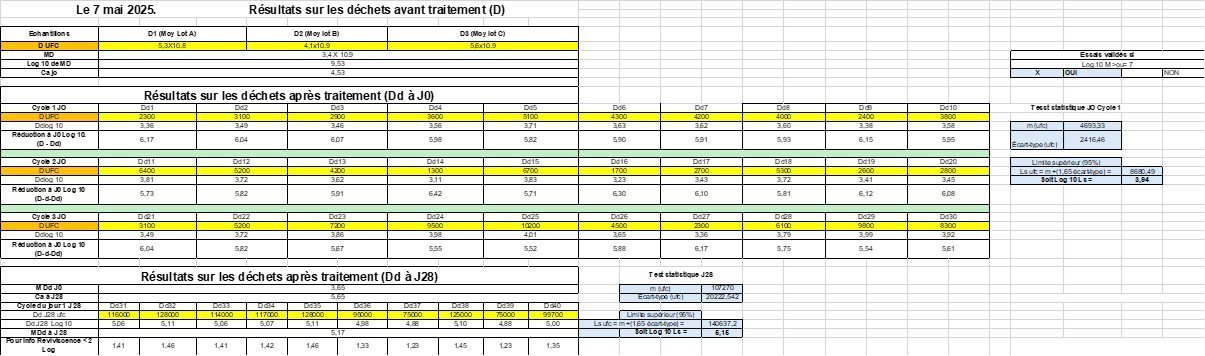
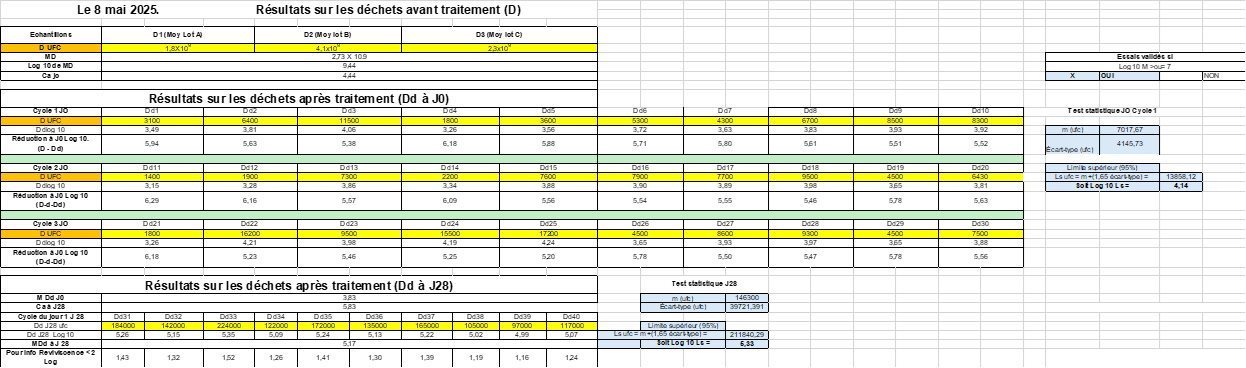
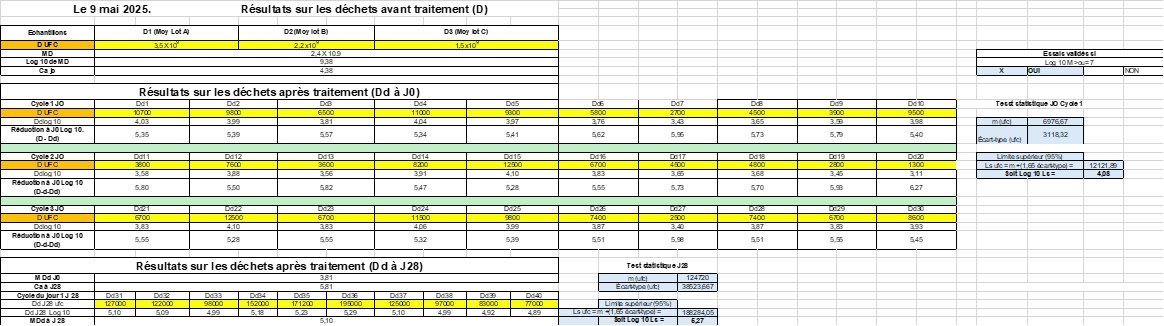
Résultats (7, 8 et 9 mai 2025)
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 7 |

|
| ➢ | Essais de granulométrie |
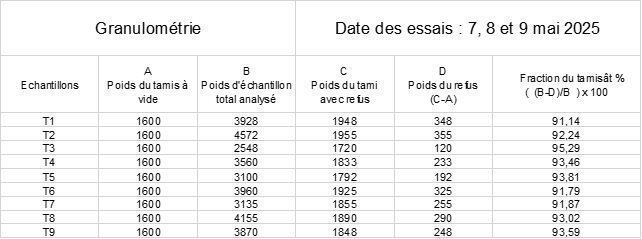
NB : la formule du tableau B5 de l’annexe A de la norme est erronée sur la colonne D (poids du refus) : (C-A)/B est à remplacer par (C-A).
Conclusion :
Les tests réalisés conformément à la norme NFX 30503-1 par le laboratoire démontrent que l’appareil de prétraitement des déchets VKIN 300 répond aux spécifications de cette norme.
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 8 |

Pr O Traoré
| Essais EC-EFRES 2025 | Laboratoire Hygiène Hospitalière CHU Clermont-Fd |
|
| 9 |